パソコンでの閲覧では一部レイアウトが崩れる場合があります。スマートフォン・タブレットでご覧いただくことを推奨しております。
問
解答
38
全圧=分圧の和より,封入した酸素の分圧は,全圧から一酸化炭素の分圧を引いた,
![]()
である。この反応前後の分圧の関係は次のように表される。
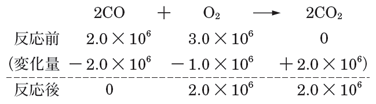
これより,反応後の酸素と二酸化炭素の分圧は,それぞれ![]() である。また,気体の場合,分圧の比と物質量の比は等しいので,反応後の酸素と二酸化炭素の物質量の比も
である。また,気体の場合,分圧の比と物質量の比は等しいので,反応後の酸素と二酸化炭素の物質量の比も![]() となる。酸素と二酸化炭素の分子量がそれぞれ,32,44であることから,混合気体の平均分子量は,
となる。酸素と二酸化炭素の分子量がそれぞれ,32,44であることから,混合気体の平均分子量は,
![]() となる。
となる。
正解へのPoint
分圧の法則(ドルトン)
分圧の法則(ドルトン)
混合気体の全圧=成分気体の分圧の和
気体の平均分子量
平均分子量=(成分気体の分子量×モル分率)の和
(例)物質量の比が![]() の空気の場合
の空気の場合
![]()